التيار الكهربائي في السوائل والغازات
التيار الكهربائي في السوائل
 في موصل معدني كهرباء يتشكل من خلال الحركة الموجهة للإلكترونات الحرة وعدم حدوث تغييرات في المادة التي يتكون منها الموصل.
في موصل معدني كهرباء يتشكل من خلال الحركة الموجهة للإلكترونات الحرة وعدم حدوث تغييرات في المادة التي يتكون منها الموصل.
تسمى هذه الموصلات ، التي لا يكون مرور التيار الكهربائي فيها مصحوبًا بتغيرات كيميائية في مادتها ، موصلات من الدرجة الأولى ... وهي تشمل جميع المعادن والفحم وعدد من المواد الأخرى.
ولكن في الطبيعة توجد أيضًا موصلات للتيار الكهربائي تحدث فيها الظواهر الكيميائية أثناء مرور التيار. تسمى هذه الموصلات الموصلات من النوع الثاني ... وهي تشتمل بشكل أساسي على محاليل مختلفة في ماء الأحماض والأملاح والقواعد.
إذا صببت الماء في وعاء زجاجي وأضفت إليه بضع قطرات من حمض الكبريتيك (أو بعض الأحماض أو القلويات الأخرى) ، ثم خذ لوحين معدنيين وربط الأسلاك بهما ، وقم بخفض هذه الألواح في الوعاء ، وقم بتوصيل تيار من المصدر إلى الأطراف الأخرى من الأسلاك من خلال المفتاح ومقياس التيار الكهربائي ، ثم يتم إطلاق الغاز من المحلول وسيستمر بشكل مستمر طالما أن الدائرة مغلقة.الماء المحمض هو في الواقع موصل. بالإضافة إلى ذلك ، ستبدأ الصفائح بالتغطية بفقاعات الغاز. ثم تنفصل هذه الفقاعات عن اللوحات وتخرج.
عندما يمر تيار كهربائي عبر المحلول ، تحدث تغيرات كيميائية تؤدي إلى إطلاق غاز.
يطلق عليهم موصلات من النوع الثاني من الإلكتروليت ، والظاهرة التي تحدث في المنحل بالكهرباء عندما يمر تيار كهربائي عبره هي التحليل الكهربائي.
تسمى الصفائح المعدنية المغمورة في المنحل بالكهرباء الأقطاب الكهربائية. أحدهما متصل بالقطب الموجب للمصدر الحالي يسمى الأنود والآخر متصل بالقطب السالب هو الكاثود.
ما الذي يحدد مرور التيار الكهربائي في موصل سائل؟ اتضح أنه في مثل هذه المحاليل (الإلكتروليتات) ، تتفكك جزيئات الحمض (القلويات والملح) تحت تأثير المذيب (في هذه الحالة الماء) إلى مكونين وجزء واحد من الجزيء له شحنة كهربائية موجبة ، والآخر أ واحد سلبي.
تسمى جزيئات الجزيء التي لها شحنة كهربائية أيونات ... عندما يذوب حمض أو ملح أو قلوي في الماء ، يحدث عدد كبير من الأيونات الموجبة والسالبة في المحلول.
يجب أن يكون من الواضح الآن سبب مرور تيار كهربائي عبر المحلول ، لأنه بين الأقطاب الكهربائية المتصلة بالمصدر الحالي ، أ التباينات المحتملةبمعنى آخر ، تبين أن أحدهما موجب الشحنة والآخر سالب الشحنة. تحت تأثير هذا الاختلاف في الجهد ، بدأت الأيونات الموجبة في الاختلاط نحو القطب السالب - الكاثود ، والأيونات السالبة - باتجاه القطب الموجب.
وهكذا ، أصبحت الحركة الفوضوية للأيونات حركة معاكسة منظمة للأيونات السالبة في اتجاه واحد والأيونات الموجبة في الاتجاه الآخر.عملية نقل الشحنة هذه عبارة عن تدفق للتيار الكهربائي عبر الإلكتروليت وتحدث طالما يوجد فرق جهد عبر الأقطاب الكهربائية. مع اختفاء فرق الجهد ، يتوقف التيار عبر المنحل بالكهرباء ، وتعطل الحركة المنظمة للأيونات وتبدأ الحركة الفوضوية مرة أخرى.
على سبيل المثال ، ضع في اعتبارك ظاهرة التحليل الكهربائي ، عندما يمر تيار كهربائي عبر محلول من كبريتات النحاس CuSO4 مع أقطاب نحاسية منخفضة فيه.
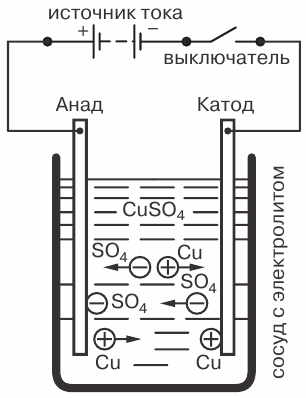
ظاهرة التحليل الكهربائي عندما يمر التيار عبر محلول من كبريتات النحاس: C - وعاء به إلكتروليت ، B - مصدر تيار ، C - مفتاح كهربائي
سيكون هناك أيضًا حركة عكسية للأيونات إلى الأقطاب الكهربائية. سيكون الأيون الموجب هو أيون النحاس (Cu) والأيون السالب سيكون بقايا الحمض (SO4). أيونات النحاس ، عند ملامستها للكاثود ، سيتم تفريغها (ربط الإلكترونات المفقودة بأنفسها) ، أي سيتم تحويلها إلى جزيئات محايدة من النحاس النقي وسيتم ترسيبها على الكاثود في شكل أنحف (جزيئي) ) طبقة.
يتم أيضًا إخراج الأيونات السالبة التي تصل إلى القطب الموجب (التبرع بالإلكترونات الزائدة). لكن في الوقت نفسه ، يدخلون في تفاعل كيميائي مع نحاس الأنود ، ونتيجة لذلك يضاف جزيء النحاس Cti إلى بقايا الحمض SO4 ، ويتشكل جزيء كبريتات النحاس CnasO4 ويعود مرة أخرى إلى بالكهرباء.
نظرًا لأن هذه العملية الكيميائية تستغرق وقتًا طويلاً ، يتم ترسيب النحاس على القطب السالب ، والذي يتم إطلاقه من الإلكتروليت. في هذه الحالة ، يستقبل المنحل بالكهرباء ، بدلاً من جزيئات النحاس التي انتقلت إلى القطب السالب ، جزيئات نحاسية جديدة بسبب انحلال القطب الموجب الثاني ، الأنود.
تحدث نفس العملية إذا تم أخذ أقطاب الزنك بدلاً من النحاس ، وكان المنحل بالكهرباء عبارة عن محلول من كبريتات الزنك ZnSO4.سينتقل الزنك أيضًا من القطب الموجب إلى القطب السالب.
لذلك ، يكمن الاختلاف بين التيار الكهربائي في المعادن والموصلات السائلة في حقيقة أن حاملات الشحنة في المعادن عبارة عن إلكترونات حرة فقط ، أي الشحنات السالبة أثناء وجود الشوارد كهرباء محمولة بواسطة جسيمات المادة المشحونة عكسيا - تتحرك الأيونات في اتجاهين متعاكسين. هذا هو السبب في أن الإلكتروليتات لها موصلية أيونية.

تم اكتشاف ظاهرة التحليل الكهربائي في عام 1837 من قبل ب. س. جاكوبي ، الذي أجرى العديد من التجارب لدراسة وتحسين المصادر الكيميائية للتيار. وجد جاكوبي أن أحد الأقطاب الكهربائية الموضوعة في محلول من كبريتات النحاس ، عندما يمر عبره تيار كهربائي ، كان مغطى بالنحاس.
تسمى هذه الظاهرة بالتشكيل الكهربائي ، والآن تجد تطبيقًا عمليًا كبيرًا للغاية. أحد الأمثلة على ذلك هو طلاء الأجسام المعدنية بطبقة رقيقة من معادن أخرى ، على سبيل المثال طلاء النيكل وطلاء الذهب والفضة وما إلى ذلك.
التيار الكهربائي في الغازات
الغازات (بما في ذلك الهواء) لا توصل الكهرباء في الظروف العادية. على سبيل المثال ، هدف أسلاك للخطوط الهوائيةعند تعليقها بالتوازي مع بعضها البعض ، يتم عزلها عن بعضها البعض بواسطة طبقة من الهواء.
ومع ذلك ، تحت تأثير درجة الحرارة المرتفعة ، وفرق الجهد الكبير وأسباب أخرى ، تتأين الغازات ، مثل الموصلات السائلة ، أي جزيئات جزيئات الغاز بأعداد كبيرة ، والتي ، كحاملات للكهرباء ، تساهم في المرور من تيار كهربائي عبر الغاز.
لكن في نفس الوقت ، يختلف تأين الغاز عن تأين موصل سائل.إذا انقسم الجزيء إلى جزأين مشحونين في سائل ، فإن الإلكترونات في الغازات تحت تأثير التأين تنفصل دائمًا عن كل جزيء ويبقى الأيون في شكل جزء موجب الشحنة من الجزيء.
على المرء فقط أن يوقف تأين الغاز ، لأنه لم يعد موصلًا ، بينما يبقى السائل دائمًا موصلًا للتيار الكهربائي. لذلك ، فإن توصيل الغاز هو ظاهرة مؤقتة ، اعتمادًا على عمل الأسباب الخارجية.

ومع ذلك ، هناك شيء آخر نوع التفريغ الكهربائييسمى تفريغ القوس أو ببساطة القوس الكهربائي. تم اكتشاف ظاهرة القوس الكهربائي في بداية القرن التاسع عشر من قبل أول مهندس كهربائي روسي في.
في أثناء إجراء العديد من التجارب ، اكتشف بتروف أنه بين فحم مرتبطين بمصدر تيار ، ظهر تفريغ كهربائي مستمر في الهواء ، مصحوبًا بضوء ساطع. في كتاباته ، كتب في. وهكذا ، لأول مرة ، تم الحصول على ضوء كهربائي ، والذي تم تطبيقه عمليًا بواسطة مهندس كهربائي روسي آخر ، بافيل نيكولايفيتش يابلوشكوف.
"Svesht Yablochkov" ، الذي يعتمد عمله على استخدام القوس الكهربائي ، أحدث ثورة حقيقية في الهندسة الكهربائية في ذلك الوقت.

يستخدم تفريغ القوس في الوقت الحاضر كمصدر للضوء ، على سبيل المثال في الأضواء الكاشفة وأجهزة العرض. تسمح درجة الحرارة العالية لتفريغ القوس باستخدامه أجهزة أفران القوس... حاليًا ، تُستخدم أفران القوس التي تعمل بتيار عالٍ جدًا في عدد من الصناعات: لصهر الفولاذ ، والحديد الزهر ، والسبائك الحديدية ، والبرونز ، وما إلى ذلك. وفي عام 1882 ، استخدم NN Benardos لأول مرة تفريغ القوس لقطع المعادن ولحامها.
في أنابيب الغاز ، ومصابيح الفلورسنت ، ومثبتات الجهد ، للحصول على حزم الإلكترون والأيونات ، ما يسمى بتفريغ غاز الوهج.
تفريغ الشرر يستخدم لقياس الفروق الكبيرة في الجهد باستخدام فجوة شرارة كروية ، يكون أقطابها كرتين معدنيتين بسطح مصقول. يتم تحريك الكرات بعيدًا ويتم تطبيق فرق جهد قابل للقياس عليها. ثم يتم تقريب الكرات من بعضها البعض حتى تمر شرارة بينهما. بمعرفة قطر الكرات والمسافة بينها وضغط الهواء ودرجة الحرارة ورطوبة الهواء ، يجدون فرق الجهد بين الكرات وفقًا لجداول خاصة. باستخدام هذه الطريقة ، يمكن قياس فرق الجهد بدقة تصل إلى بضعة في المائة لترتيب عشرات الآلاف من الفولتات.
